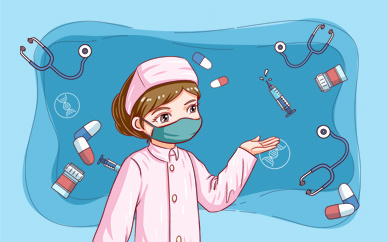
浙江大学展示的国内首例厘米级细胞培养大黄鱼组织仿真鱼排样品。洪恒飞 摄
 (资料图片仅供参考)
(资料图片仅供参考)
从液氮中取出保藏好的大黄鱼干细胞“种子”,利用细胞活化及可控生长路径合成鱼肉,满足一次鱼肉消费。原本有限的大黄鱼供应,其可持续生产变得无限可能……随着细胞培养肉类技术的成熟,这一场景或许并不会仅局限于想象。
不久前,由浙江大学生物系统工程与食品科学学院副院长刘东红教授、生命科学学院陈军教授牵头的科研团队联合大连工业大学朱蓓薇院士团队对外宣布,联合团队通过干细胞分离、工厂化培养与组织化构建技术,耗时17天成功合成国内首例厘米级细胞培养大黄鱼组织仿真鱼排。
细胞培养肉被认为是极有潜力解决未来人类餐桌肉品和蛋白供应、减少人工养殖肉类动物对水资源、土地资源高度依赖的技术之一。牛肉、鸡肉、鹅肝、猪肉、鱼肉……近十年来,基于不同生物的细胞培养肉接连问世,公众在惊叹培养技术之余,同样关心口味、价格、安全性等影响消费的因素。
刘东红对此表示,多种肉类的培养体系慢慢涌现,一方面需要尽快实现低成本和规模化生产,一方面需要健全法律法规、评估安全性。值得期待的是,全球范围内,技术与应用正在同步推进。
一场直播掀起了研发热潮
2013年,一场位于英国伦敦的特殊烹饪直播,令细胞培养肉类食品引起广泛关注——彼时,荷兰马斯特里赫特大学组织工程学教授马克·波斯特利用从牛颈提取的一种称为“肌卫星细胞”的特殊干细胞,耗时数周完成了全球首例体外培养出的细胞培养肉,并通过烹饪直播向公众展示。
“这十年间,多国科研人员纷纷参与到细胞培养肉这一领域。实际上,细胞培养技术本身并不算新鲜事物。”刘东红介绍,半个多世纪前,医学上已开始细胞培养人体组织工程的研究,用于皮肤修复等。进入21世纪,国际社会越发关注粮食供应、资源紧缺的问题,利用体外细胞来培养蛋白质或者肌肉纤维的相关技术逐渐酝酿。
刘东红解释说,细胞培养肉,本质上是通过动物干细胞在体外进行细胞增殖和分化的过程。其中,细胞通过增殖不断增加数量,再通过分化产生形态结构功能各异的细胞类群或组织,如肌肉组织。
虽然公众对细胞培养肉普遍持观望态度,但局部范围内已有人敢于试吃,其产业化前景也被资本市场所看好。近日,在第十九届畜牧饲料科技与经济(全球)高层论坛上,南京农业大学周光宏教授介绍,根据国外机构统计,细胞培养肉行业年度投资(2016-2021年)总计19.3亿美元,其中2021年投入资本13.8亿元,比2019年上涨300%以上。
近两年,已有美国FDA和新加坡食品管理局批准细胞培养鸡肉上市的事例。2021年,Future Meat Technologies公司宣布其中试车间在以色列竣工,可达到日产500千克细胞培养肉。
回顾国内,2019年11月,周光宏团队发布国内首例细胞培养猪肉。同年,由周光宏任首席科学家的科技企业南京周子未来食品科技有限公司注册成立。今年4月,周子未来宣布完成数千万元人民币的A+轮融资,将促进该公司落地细胞培养肉种子细胞千升规模的中试工厂。
在刘东红看来,资本与技术相互交融,正有效加快这一领域的产业化进程。
选好“种子”与“土壤”极为关键
5月23日,科技日报记者走进位于浙江嘉善的浙大长三角智慧绿洲创新中心未来食品实验室,只见展厅内摆放着一块瓶盖大小、泛着油光的鱼肉,凑近一看能观察到鱼肉表面细致的纹理,甚至淡淡的腥味。这便是国内首例厘米级细胞培养大黄鱼组织仿真鱼排样品。
刘东红告诉记者,不同肉类的细胞培育方法大同小异,难点在于找到合适的细胞系与构建培养基,二者相当于种子和土壤的关系。
以仿真鱼排为例,科研人员从大黄鱼轴上肌和腹侧体腔脂肪中筛选分离出肌肉干细胞和脂肪干细胞,作为细胞培养鱼肉的“种子”,并通过调控两种信号通路诱导肌肉干细胞分化。
之所以将培养基比作土壤,是因为需要通过它将氨基酸、葡萄糖等能支持细胞增殖分化的基本营养素和多种生长因子组合,为细胞增殖分化提供养分。
随着肌肉细胞的生长、分化,越来越多的鱼肉产生,但鱼肉还只是肉泥。怎么把鱼肉搭建起来?联合团队基于可食用凝胶改造仿生构建鱼肌支架,产生类似自然鱼肉该有的结构和纹路,令肌肉细胞沿着3D打印的仿生结构有规则地生长,让仿真鱼排得以成形。
陈军表示,培养基是细胞培养肉生产流程中最重要的成本控制环节,联合团队筛选得到了低血清的基础培养基,有效控制成本,为后续大规模化生产打下基础。
去年5月,清华大学医学院杜亚楠教授课题组在《生物材料》发表研究论文,介绍团队在可食用的多孔明胶微型生物支架上,利用生物组装技术培养出数厘米大小的人造肉丸。其中,微载体的立体多孔结构,比传统的2D细胞培养瓶更加节省培养基的用量,从而降低了人造肉丸的成本。
“相比发达国家,尽管我国在这一领域起步稍有落后,但是近几年迎头追赶,与国际前沿水平基本实现并跑。”刘东红说,从丰富种类、降低成本等维度开展创新,新的技术发现还会持续涌现。
从展厅到餐厅需要双线推进
今年3月,联合国粮食及农业组织和世界卫生组织发布了一份题为《细胞基食品的食品安全问题》的全球报告。该报告指出,预计到2050年,世界人口将达到90亿—110亿,随之而来的是蛋白质需求增长以及潜在的健康和环境问题。
根据周光宏团队推算,理论上,1克肉上提取的干细胞,经过7周、分裂45次,可以培养出2万千克重的培养肉。
诚然,要实现这一体量,还有相当长的一段路要走。在他看来,细胞培养肉成本需降到每克0.03元,有可能实现对畜牧肉类的部分替代。
刘东红认为,细胞培养肉的研发初衷,并非要马上替代现有的食品,更重要的是作为一种技术布局防患于未然。时下我国主要江河湖海处于禁渔期,就是为了保护自然提供的水生资源,维持生态平衡,实现可持续发展。
“同时,国内开展相关研发布局,有利于在未来掌握主动权。”刘东红说,针对影响细胞培养肉类安全性的风险物质,团队已启动若干研究项目,以期在该领域的国际竞争中争取话语权。
该报告提到,考虑到细胞基食品技术的快速发展,各国需要做好充分准备建立必要的监管框架、监管机构和基础设施,以评估细胞基食品产品和生产过程的安全性,并为销售这些产品的公认术语和标签要求制定法律和法规。
虽然尚未大范围普及,但细胞培养肉的关注度之高,好似已置身于阳光厨房。
“相关法律法规、监管体系的健全必然有一个过程。”刘东红说,在此期间,科研人员与业界需要围绕降低成本和确保安全性,进一步深化研究,为规模化生产做准备。比如,寻找培养基中高成本生产因子的可替代物、提升细胞繁殖和分化速度的关键因子等。
周光宏表示,细胞培养肉技术将重塑肉品产业格局,即未来的食用肉,一部分由畜牧业生产,一部分通过养细胞得到,还有一部分则是植物蛋白仿真肉。确保营养、安全、好吃,细胞培养肉自然而然会被接受。